腫瘤相關(guān)巨噬細胞(Tumor-associated macrophages,TAMs)是免疫抑制性腫瘤細胞微環境(Immunosuppressive tumor microenvironment,TME)中主要的成分(fēn),包括兩大類的巨噬細胞,M1和M2型巨噬細胞。其中M2型占大多數,這(zhè)些(xiē)巨噬細胞通過分(fēn)泌生(shēng)長因子(zǐ)、基質降解酶和促血管生(shēng)成因子(zǐ)等多種機制支持腫瘤生(shēng)長。此外,還通過産生(shēng)一(yī)系列抗炎細胞因子(zǐ)(如(rú)IL-10)和消耗T細胞功能(néng)所必需氨基酸的酶(如(rú)Arginase 1)抑制免疫細胞,或通過表達抑制性免疫檢查點配體(tǐ)(如(rú)PDL1)等多種方式促進腫瘤的生(shēng)長。而M1型巨噬細胞的功能(néng)與M2型相反,它可以抑制腫瘤的生(shēng)長,協同其他免疫細胞發揮抗腫瘤的免疫功能(néng)。基于此,在TME中對TAMs重編程,是一(yī)種有效抗腫瘤策略。
目前包括CAR-T在内的新(xīn)一(yī)代治療策略可對TME進行重新(xīn)編程。相較于常規性的直接靶向腫瘤細胞的CAR-T療法,新(xīn)一(yī)代CAR-T則是靶向TME中的非腫瘤成分(fēn),間(jiān)接地限制了(le)腫瘤的發生(shēng)發展。
今年Daniel J. Powell Jr團隊在Nature Communications上(shàng)發表了(le)一(yī)篇題為(wèi)“CAR-T cell-mediated depletion of immunosuppressive tumor-associated macrophages promotes endogenous antitumor immunity and augments adoptive immunotherapy”的文章。該研究團隊主要利用CAR-T耗盡FRβ+TAMs(表達FRβ的TAMs亞群具有M2型巨噬細胞表型和功能(néng)),最終導緻TME的重編程,促進内源性T細胞介導的抗腫瘤作(zuò)用。

FRβ(葉酸受體(tǐ)β)是一(yī)種在急性髓樣白血病細胞中表達的糖磷脂酰肌醇錨定的受體(tǐ),目前已成為(wèi)CAR-T細胞療法的腫瘤抗原靶标。該研究團隊首先驗證了(le)卵巢癌組織中FRβ的表達,發現(xiàn)當腫瘤生(shēng)長到有腹水形成時(shí),FRβ+TAMs亞群占到了(le)巨噬細胞總數的52.14 ± 11.42%,并且FRβ+TAMs亞群并不是一(yī)個(gè)靜止的狀态,而是一(yī)個(gè)随着腫瘤生(shēng)長不斷增加的亞群;此外,正常小鼠的巨噬細胞在腫瘤細胞培養上(shàng)清中培養24h,其FRβ的表達也(yě)明顯增加。
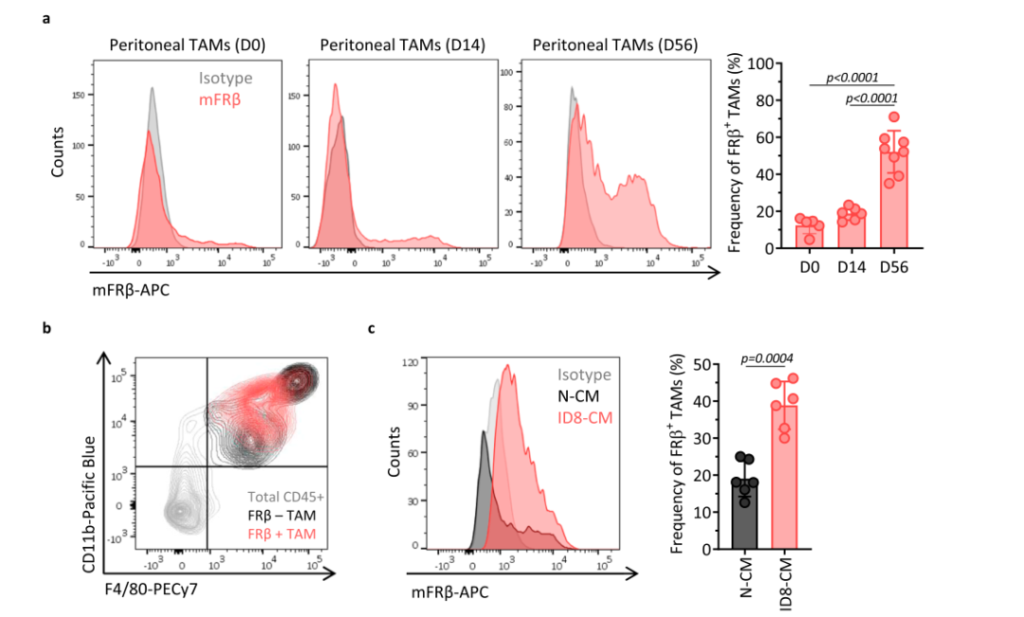
之後,該研究團隊利用免疫熒光進一(yī)步證實了(le)FRβ+TAMs形态與M2型巨噬細胞一(yī)緻,FRβ–TAMs形态與M1型巨噬細胞一(yī)緻。此外,FRβ+TAMs表面高表達CD204,CD206和CD163,與M2表型基本一(yī)緻。采用多重細胞因子(zǐ)分(fēn)析法發現(xiàn)FRβ–TAMs分(fēn)泌IL-6,IL-27,IL-17α,TNF-α,IFN-β和GM-CSF的能(néng)力高于FRβ+TAMs;而FRβ+TAMs高分(fēn)泌IL-10。并且這(zhè)種能(néng)力在LPS的刺激下(xià)可進一(yī)步增強。
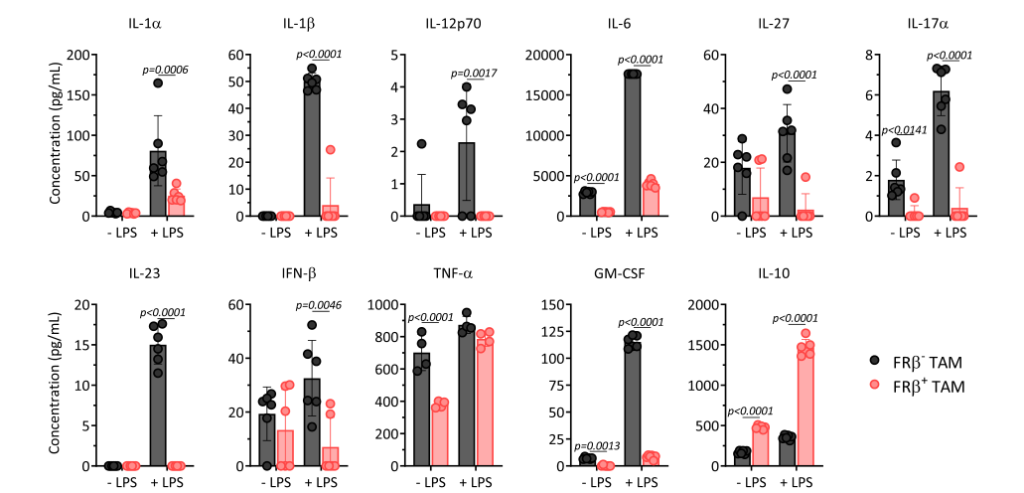
接着,該研究團隊驗證了(le)具有M2表型的FRβ+TAMs對T細胞的抑制作(zuò)用。利用小鼠特異性人(rén)間(jiān)皮素(hMeso)的CAR-T 細胞建立了(le)抗原特異性T細胞反應模型。用細胞示蹤染料标記hMeso CAR-T細胞,并與工程化(huà)的ID8.hMeso細胞共培養,在共培養初期加入分(fēn)選的 FRβ+或FRβ–TAMs。結果發現(xiàn),在FRβ+TAMs存在下(xià),hMeso CAR-T的增殖及分(fēn)泌IFN-γ的能(néng)力明顯低(dī)于加入FRβ–TAMs的情況。
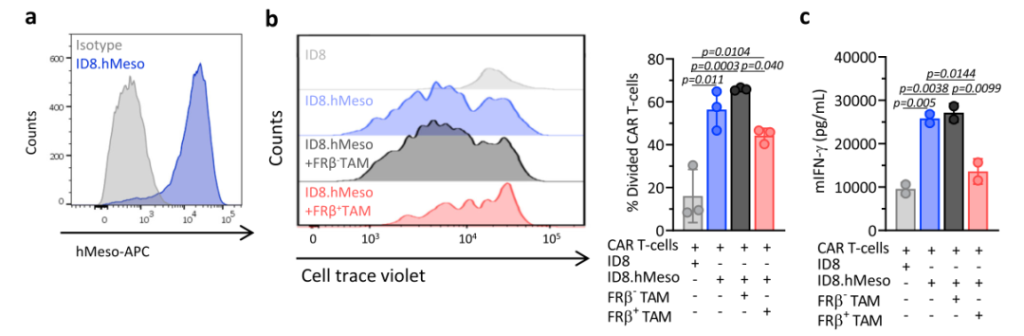
CAR-T細胞療法已經介導了(le)針對不同抗原的某些(xiē)類型的癌症的完全緩解。基于此,該研究團隊構建了(le)針對FRβ靶點的CAR-T。之後,研究團隊從負荷ID8腫瘤的Folr2 wt和Folr2-/-(敲除FRβ基因)小鼠的腹水中分(fēn)離CD11b+細胞與構建好(hǎo)(hǎo)的CAR-T體(tǐ)外共培養。結果顯示,mFRβ CAR-T與Folr2 wt小鼠的TAMs共培養時(shí)才能(néng)分(fēn)泌更高水平的IFN-γ和更強的誘導靶細胞裂解的能(néng)力。
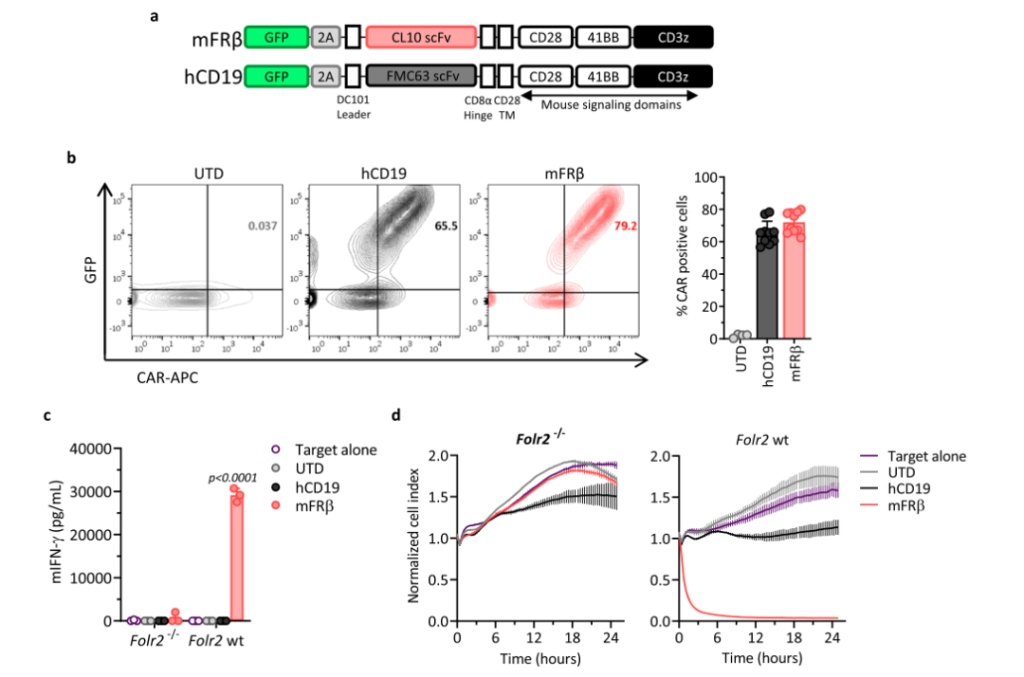
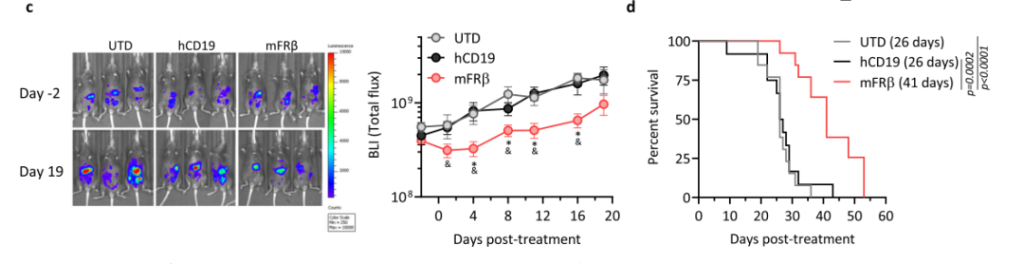
然後,研究團隊在ID8小鼠模型中進一(yī)步驗證了(le)mFRβ CAR-T的作(zuò)用。發現(xiàn)mFRβ CAR-T細胞導緻FRβ+TAMs的耗竭,TME中招募大量的免疫細胞,包括CD11b+細胞和CD8+T細胞。而内源性腫瘤特異性CD8+T細胞的大量湧入,最終抑制了(le)腫瘤的生(shēng)長并延長了(le)生(shēng)存時(shí)間(jiān)。
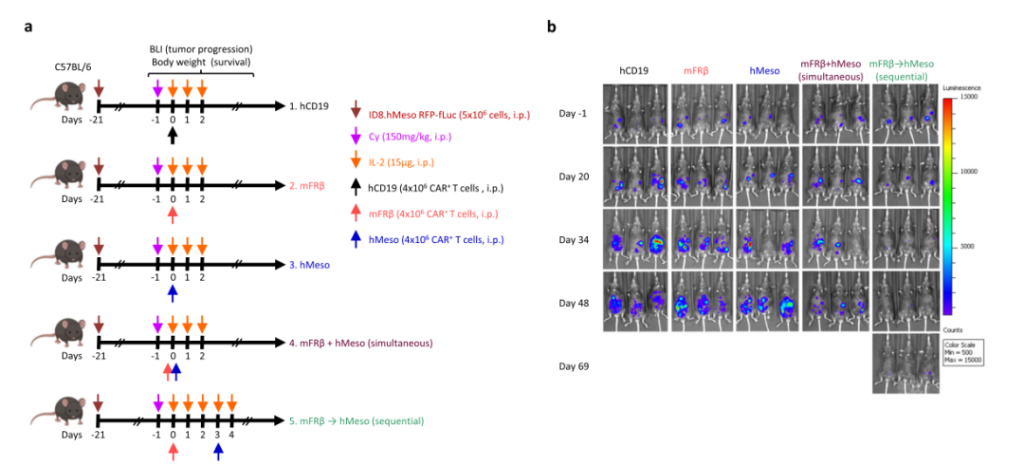
同樣的,通過FRβ特異性CAR-T細胞對TME進行預處理(lǐ)也(yě)可以提高腫瘤導向性的抗間(jiān)皮素CAR-T細胞的效果,而同時(shí)使用以上(shàng)兩種CAR-T細胞則不能(néng)産生(shēng)相應的效果。接着,研究團隊研究了(le)mFRβ CAR-T聯合傳統靶向腫瘤的CAR-T療法是否能(néng)夠增強抗腫瘤效果。為(wèi)此,在C57BL/6小鼠接種ID8.hMeso腫瘤細胞,21天後,将小鼠随機分(fēn)成4組(hCD19,mFRβ,hMeso以及mFRβ+hMeso CAR-T)。發現(xiàn)兩種CAR-T聯合使用并不能(néng)提高抗腫瘤效果;而事(shì)先通過mFRβ CAR-T細胞對TME進行預處理(lǐ)後,可以提高腫瘤特異性的hMeso CAR-T細胞的效果,延長小鼠的生(shēng)存期。此外,利用mFRβ CAR-T預處理(lǐ)後,可以增強小鼠血液中hMeso CAR-T的濃度。
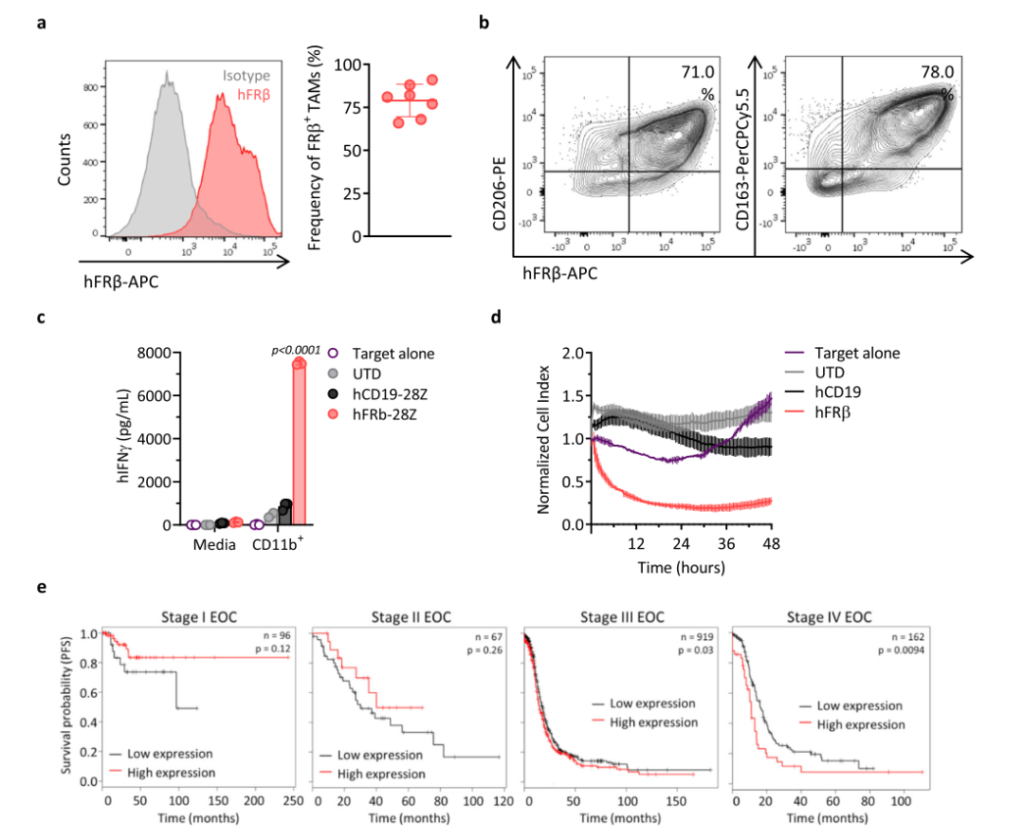
之後,該研究團隊檢測了(le)臨床腫瘤樣本中FRβ+TAMs,發現(xiàn)幾乎所有的腫瘤組織中都存在高比例的FRβ+TAMs,并且FRβ和CD206,CD163共表達,這(zhè)與在小鼠中發現(xiàn)的類似。此外,采用磁珠法從人(rén)腹水中分(fēn)離 CD11b+細胞,與不同的CAR-T共培養,發現(xiàn)在hFRβ CAR-T 細胞中觀察到抗原特異性IFN-γ 的産生(shēng)和 CD11b+ 細胞(含FRβ+TAMs)的特異性溶解。這(zhè)為(wèi)建立CAR-T靶向hFRβ TAMs提供了(le)可行性。最後,為(wèi)了(le)探討(tǎo)FRβ 在卵巢癌患者中的臨床意義,該研究團隊研究了(le)FRβ 基因的表達與無進展生(shēng)存期(PFS)的相關(guān)性。發現(xiàn),雖然在卵巢癌早期(Ⅰ和Ⅱ期)患者中沒有觀察到明顯的相關(guān)性,但(dàn)是在Ⅲ期和 Ⅳ期表達高 FOLR2的患者與表達低(dī)的患者相比,中位生(shēng)存期明顯縮短。并且在其他腫瘤患者中也(yě)顯示相同的結果。這(zhè)揭示了(le)重要的預後價值,同時(shí)也(yě)支持了(le)靶向表達FRβ 免疫抑制性巨噬細胞在癌症患者中的潛在益處。
綜上(shàng),該研究團隊開發了(le)一(yī)種針對TAMs的CAR-T,可以将TME重編程為(wèi)一(yī)個(gè)促進抗腫瘤免疫反應和限制腫瘤進展的TME,提高其他免疫療法的療效,包括CAR-T細胞療法。以前的研究主要是用單克隆抗體(tǐ)或者小分(fēn)子(zǐ)藥物來(lái)靶向TAMs,然而這(zhè)種策略需要持續給藥,以防止巨噬細胞再次的增殖,并且也(yě)容易發生(shēng)全身(shēn)性細胞毒性;而FRβ CAR-T具有增殖能(néng)力,能(néng)夠在較長時(shí)間(jiān)存在,并且安全性也(yě)是比較好(hǎo)(hǎo)的。總之,利用CAR-T靶向免疫抑制性細胞是一(yī)種非常有潛力的治療方法。
