過去十年免疫療法的發展,改變了(le)腫瘤治療的模式。但(dàn)是,多數患者仍然沒有受益于免疫療法,這(zhè)可能(néng)與免疫抑制的腫瘤微環境(TME)相關(guān)。腫瘤細胞的代謝調節不僅在維持腫瘤生(shēng)長方面起着重要的作(zuò)用,而且其代謝産物也(yě)會影響免疫細胞的作(zuò)用,導緻免疫細胞營養供給不足,代謝失調,進而導緻酸性的腫瘤微環境,影響免疫細胞的作(zuò)用。通過靶向代謝藥物,可以進一(yī)步重編程TME,增強抗腫瘤免疫反應。
該篇綜述”Navigating metabolic pathways to enhance antitumour immunity and immunotherapy”主要介紹了(le)影響抗腫瘤免疫反應的代謝途徑及靶向代謝途徑的藥物,以增強免疫反應。
代謝是生(shēng)物體(tǐ)内所發生(shēng)的用于維持生(shēng)命活動的一(yī)系列有序的化(huà)學反應的總稱,這(zhè)些(xiē)反應不僅可以産生(shēng)個(gè)體(tǐ)生(shēng)存和維持細胞功能(néng)所需的能(néng)量,而且可以保持生(shēng)物體(tǐ)的結構,及時(shí)對外界環境做出反應。代謝途徑與細胞信号,表觀遺傳等密切相關(guān),因此代謝途徑在細胞穩定,響應細胞内外刺激時(shí)發揮重要作(zuò)用。
1. 糖代謝
異常的生(shēng)物能(néng)量活動使得腫瘤細胞攝取大量的葡萄糖,通過糖酵解途徑産生(shēng)乳酸,即使在有氧條件下(xià),也(yě)會産生(shēng)大量乳酸,同時(shí)氧化(huà)磷酸化(huà)的速率降低(dī)。這(zhè)種現(xiàn)象被稱為(wèi)Warburg效應。乳酸在細胞中的積累,激活細胞膜上(shàng)的單羧酸鹽轉運蛋白(MCT),特别是單羧酸鹽轉運蛋白(MCT4),而這(zhè)種轉運蛋白可以将乳酸運送到細胞外環境,導緻酸性腫瘤微環境,抑制腫瘤免疫以促進腫瘤的發展。
此外,乳酸的大量積累,也(yě)會導緻TILs的mTOR活性降低(dī),NFAF信号和及糖酵解能(néng)力降低(dī),最終導緻抗腫瘤效應分(fēn)子(zǐ)活性受損,抗腫瘤免疫反應降低(dī)。特别是嚴重影響了(le)T細胞介導的抗腫瘤免疫應答(dá)及TILs的活率(圖1)。酸性的腫瘤微環境利于腫瘤免疫細胞的發育,包括耐受性的DCs,M2樣巨噬細胞和MDSC等;而不利于DC和M1型巨噬細胞的成熟和分(fēn)化(huà)。此外,乳酸還會影響NK細胞的功能(néng),影響IFNγ的分(fēn)泌。實際上(shàng),腫瘤細胞産生(shēng)的乳酸還可以通過促進IL-23和IL-17介導的的炎症反應而促進腫瘤的生(shēng)長。除調節免疫應答(dá)外,腫瘤細胞可以将腫瘤相關(guān)成纖維細胞(CAF)産生(shēng)的乳酸作(zuò)為(wèi)自身(shēn)生(shēng)長的能(néng)量來(lái)源。
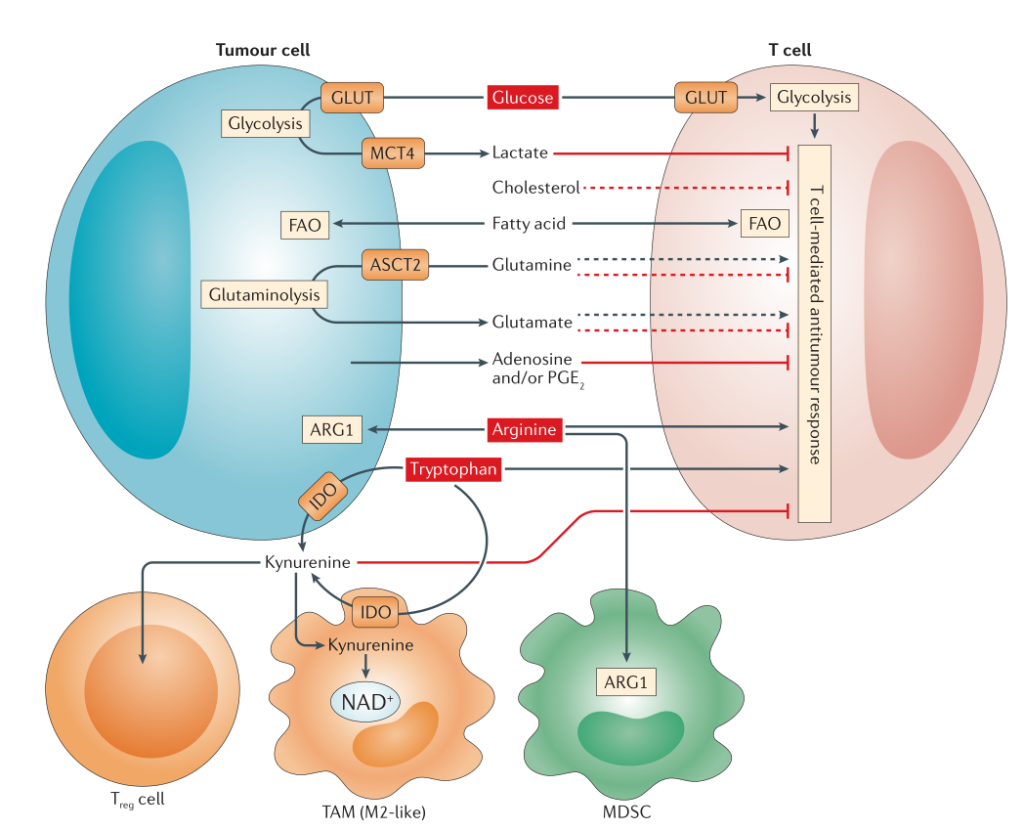
若幹臨床研究結果表明,腫瘤中有氧糖酵解活性與宿主抗腫瘤免疫反應和抗腫瘤免疫療法的治療結果呈負相關(guān)。例如(rú),對于過繼性T細胞療法(ACT)不敏感的腫瘤,具有更高的糖酵解活性;對黑色素瘤患者進行相幹檢測發現(xiàn),乳酸脫氫酶A(LDHA)和乳酸的表達水平與T細胞活性和患者的整體(tǐ)生(shēng)存率呈現(xiàn)負相關(guān)。這(zhè)些(xiē)結果表明糖酵解活動不僅為(wèi)腫瘤細胞的生(shēng)長提供了(le)能(néng)量,而且還可以幫助腫瘤細胞免疫逃逸。
基于此,靶向葡萄糖代謝和乳酸産生(shēng)和分(fēn)泌是抗腫瘤治療的有效策略。例如(rú),PFKFB3(可以促進腫瘤中的糖酵解活性和乳酸的産生(shēng))抑制劑已被證明,可以消除Warburg效應,減少腫瘤進展和轉移。FX11(LDHA抑制劑)可以降低(dī)腫瘤生(shēng)長。此外,也(yě)有靶向糖酵解藥物與免疫檢查點抑制劑聯合治療腫瘤。例如(rú),PKM2(在糖酵解過程中可以将磷酸丙酮酸轉化(huà)為(wèi)丙酮酸的酶)可以聯合PD-1或PDL1抑制劑來(lái)增強抗腫瘤免疫反應。這(zhè)些(xiē)結果共同表明,通過減少乳酸的産生(shēng)可以增強抗腫瘤免疫療法的療效。但(dàn)是,靶向糖酵解是一(yī)把雙刃劍,一(yī)方面會對包括T細胞,NK細胞等在内的免疫細胞産生(shēng)影響,抑制其功能(néng),另一(yī)方面也(yě)會抑制由IL-7,IL-6和IL-23介導的促腫瘤反應。因此需要綜合考慮,确保持續有效的抗腫瘤反應。同時(shí)需要探索腫瘤發生(shēng)不同階段糖酵解途徑,以便使用合适的靶向藥物。
2.基酸代謝
2.1谷氨酰胺和谷氨酸
谷氨酰胺在維持細胞生(shēng)長過程中起着重要作(zuò)用,在缺乏能(néng)量情況下(xià),腫瘤細胞也(yě)可以通過谷氨酰胺途徑獲取細胞生(shēng)存能(néng)量。其代謝産物如(rú)谷氨酸,α-KG和天冬氨酸可以調節細胞代謝,表觀遺産學,核苷酸合成和氧化(huà)還原反應等。此外,糖酵解活動也(yě)會影響谷氨酰胺的代謝。糖酵解的代謝産物乳酸可以通過誘導HIF2α的表達,促進谷氨酰胺轉運蛋白(ASCT2)和谷氨酰胺酶1(GLS)的表達,以此誘導腫瘤中谷氨酰胺分(fēn)解的增加(圖1)。此外,谷氨酰胺對于維持免疫應答(dá)也(yě)發揮着重要的作(zuò)用。活化(huà)的T細胞和巨噬細胞通過上(shàng)調谷氨酰胺的表達,增加免疫應答(dá)的能(néng)力。谷氨酰胺的缺乏可以抑制T細胞的活化(huà)和細胞因子(zǐ)的産生(shēng)。因此,靶向谷氨酰胺成為(wèi)治療腫瘤的另一(yī)個(gè)有效策略。但(dàn)是,靶向谷氨酰胺代謝的幹預措施同時(shí)影響TME和抗腫瘤免疫的狀态,需進一(yī)步确定谷氨酰胺如(rú)何調控TME細胞中谷氨酰胺代謝以及谷氨酰胺調控T細胞的潛在機制,有利于靶向藥物的研發。目前CB-839是比較理(lǐ)想的藥物,正在實體(tǐ)瘤和血液腫瘤中進行相關(guān)臨床試驗。
2.2 精氨酸
精氨酸的代謝在T細胞活化(huà)和調節免疫應答(dá)中起着關(guān)鍵的作(zuò)用。在TME中聚集了(le)表達精氨酸酶1(ARG1)免疫調節細胞,包括M2樣的巨噬細胞(TAMS),DC和Treg細胞,可以通過降解精氨酸并限制T細胞的攝取,從而抑制抗腫瘤免疫反應。此外,有研究發現(xiàn),額外補充精氨酸可以刺激T細胞和NK細胞的細胞毒活性和效應細胞因子(zǐ)的産生(shēng),聯合PD-1抗體(tǐ),可以進一(yī)步增強小鼠的抗腫瘤免疫能(néng)力,延長小鼠生(shēng)存期。因此增加精氨酸分(fēn)泌和防止精氨酸在TME中降解是重新(xīn)激活T細胞和NK細胞介導免疫應答(dá)的非常具有吸引力的策略之一(yī)。目前AGR1抑制劑INCB001158聯合pembrolizumab正在進行臨床試驗。
2.3 色氨酸
色氨酸是生(shēng)物體(tǐ)進行蛋白質合成和生(shēng)物代謝所必需的氨基酸之一(yī)。生(shēng)物體(tǐ)内一(yī)般通過兩種色氨酸降解酶(吲哚胺2,3-二氧化(huà)酶(IDO)和色氨酸2,3-二氧化(huà)酶(TDO)),可以将色氨酸分(fēn)解為(wèi)犬尿氨酸,并為(wèi)NAD+合成提供原料。而腫瘤細胞高表達色氨酸降解酶,導緻腫瘤的發展并抑制T細胞的抗腫瘤能(néng)力(圖1)。此外,有研究發現(xiàn),減少IDO的表達可以減少M2型巨噬細胞;IDO沉默的DC細胞可以增加抗原特異性的T細胞的增殖和細胞毒活性,促進腫瘤特異性T細胞的活化(huà)。基于此,IDO的抑制劑是增強抗腫瘤應答(dá)的一(yī)種比較有前途的方法。
目前IDO抑制劑聯合CTLA-4抗體(tǐ)(ipilimumab)正在進行臨床試驗,用于評估在黑色素瘤患者中的療效。總之,評估腫瘤中IDO的表達水平,及治療前的IDO表達與T細胞浸潤的關(guān)系,可能(néng)是優化(huà)這(zhè)種方法的關(guān)鍵。在這(zhè)裏需要注意的一(yī)點是,在TME中IDO抑制劑會損害NAD+的産生(shēng),而NAD+是維持T細胞免疫反應關(guān)鍵的物質。因此在使用IDO抑制劑時(shí)需要綜合考慮。
2.4 其他
此外,2-羟基戊酸鹽,亞甲基丁二酸和PGE2途徑都與TME中免疫細胞的抗腫瘤反應密切相關(guān)。例如(rú),大部分(fēn)膠質瘤細胞高表達異檸檬酸脫氫酶1(IDH1)或IDH2的突變體(tǐ),促進腫瘤的發生(shēng),抑制T細胞的浸潤。目前IDH1抑制劑聯合Nivolumab正在進行臨床試驗。
3. 脂肪酸代謝
腫瘤細胞通常具有較高的脂肪酸合成速率,這(zhè)樣可以為(wèi)磷脂和信号分(fēn)子(zǐ)的生(shēng)成提供能(néng)量。此外,脂肪酸合成可以為(wèi)免疫細胞增殖提供細胞膜和其他關(guān)鍵的脂質細胞結構,也(yě)是炎症巨噬細胞分(fēn)化(huà)和功能(néng)所必需的。例如(rú),有效的TCR聚集和形成免疫突觸對于T細胞功能(néng)是至關(guān)重要,而這(zhè)依賴于細胞膜的脂質組分(fēn)。不同的脂肪酸對CD4+T細胞增殖和分(fēn)化(huà)發揮不同的功能(néng)。如(rú),長鏈脂肪酸促進CD4+T向TH1和Th17細胞分(fēn)化(huà),而短鏈脂肪酸促使CD4+T向Treg細胞分(fēn)化(huà)。因此TME中脂肪酸的類型決定了(le)其浸潤的CD4+T細胞的類型及其抗腫瘤作(zuò)用。
脂肪的累積會使腫瘤浸潤的免疫細胞(包括MDSC,DC和TAMS)通過代謝的重編程向免疫抑制和抗炎型表型分(fēn)化(huà)。這(zhè)些(xiē)發現(xiàn)共同表明,TME中脂質代謝在協調免疫抑制和通過靶向代謝途徑提高抗腫瘤免疫能(néng)力中發揮着重要功能(néng),為(wèi)提高機體(tǐ)抗腫瘤免疫能(néng)力提供了(le)一(yī)個(gè)新(xīn)的策略。
4. 訓練型免疫力
訓練型的免疫力是一(yī)種特别的免疫反應,它可以通過訓練刺激物,如(rú)β-葡聚糖,長期提高先天免疫細胞的活性,并通過代謝誘導表觀遺傳的重編程。考慮到先天免疫細胞在免疫抑制TME形成過程中的重要作(zuò)用,在TAMs和腫瘤浸潤DCs中,刺激訓練免疫通過重編程TME代謝,使其更具免疫刺激作(zuò)用,從而能(néng)夠與其他免疫療法産生(shēng)協同作(zuò)用,如(rú)α-KG、乙酰輔酶A等。這(zhè)種訓練刺激已在不同試驗中得到應用,其目的是引起抗腫瘤反應。
5. 免疫檢查點
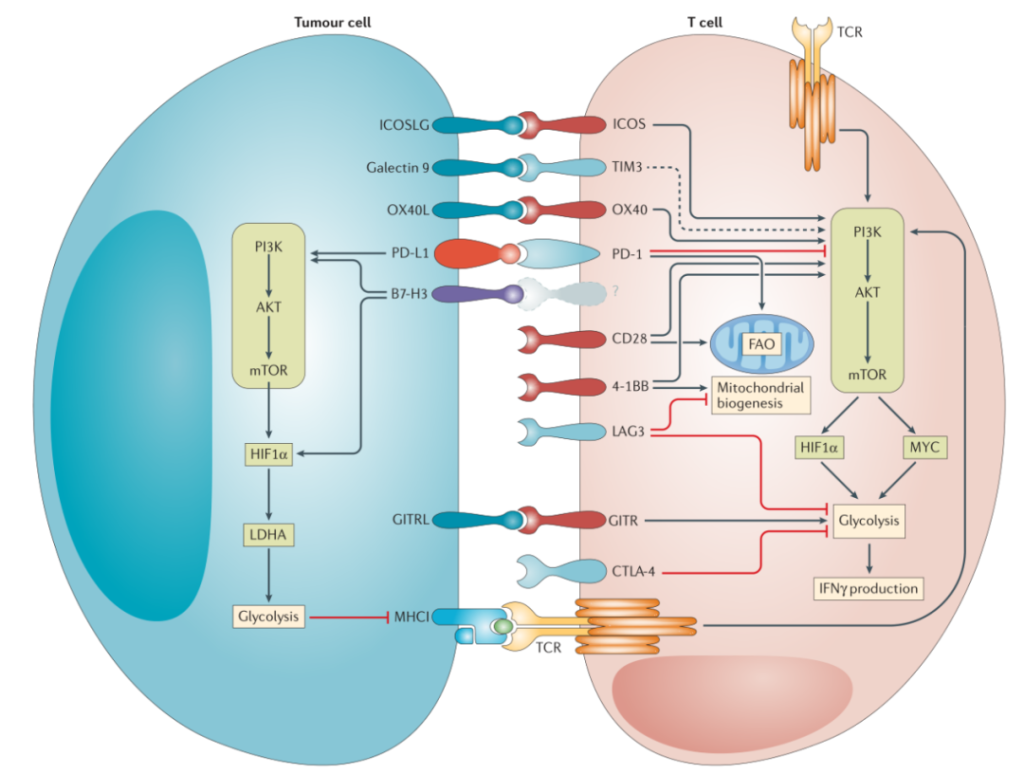
ICIs是腫瘤治療比較有效的方法,通過增強T細胞活化(huà)信号通路(lù)從而增強抗腫瘤能(néng)力,但(dàn)是新(xīn)的證據表明,ICIs也(yě)會影響T細胞的代謝(圖2)。例如(rú),PD1與配體(tǐ)PDL1或PDL2結合,通過抑制PI3K-AKT-mTOR信号而影響代謝的重編程,包括有氧糖酵解和谷氨酰胺分(fēn)解的上(shàng)調。因此抑制PD1/PDL1信号通路(lù),可以促使TILs的重新(xīn)活化(huà)和代謝适應,同時(shí)抑制腫瘤細胞中的有氧糖酵解,從而起到協調的抗腫瘤作(zuò)用。與抑制性免疫檢查點受體(tǐ)引起的代謝損傷相反,協同刺激分(fēn)子(zǐ)通過轉錄重編程和代謝開關(guān)的信号通路(lù)來(lái)維持T細胞的活化(huà)。例如(rú),CD28信号通過同時(shí)刺激有氧糖酵解和促進線粒體(tǐ)融合,從而有效地産生(shēng)乙酰輔酶A來(lái)增強T細胞的代謝 (圖2)。類似地,4-1BB信号傳導,極大的增強了(le)CD8+T細胞增殖,同時(shí)激活葡萄糖和脂肪酸代謝。目前,越來(lái)越多的證據表明共刺激受體(tǐ)對T細胞代謝會産生(shēng)的重大影響。因此ICIs和協調刺激分(fēn)子(zǐ)的聯合療法是另一(yī)種比較有前途的治療方法。
6. T細胞的線粒體(tǐ)調節
TCR刺激能(néng)夠誘導線粒體(tǐ)的重塑,這(zhè)是滿足T細胞活化(huà)的代謝需求所必需的。TCR活化(huà)還能(néng)刺激線粒體(tǐ)反應性樣物質(ROS)的生(shēng)成,同時(shí)又可以驅動T細胞活化(huà)。
過氧化(huà)物酶體(tǐ)增殖物激活受體(tǐ)γ共激活因子(zǐ)1 (PGC-1α )是核激素受體(tǐ)過氧化(huà)物酶體(tǐ)增殖物激活受體(tǐ)γ( PPARγ)的轉錄共激活因子(zǐ),廣泛參與線粒體(tǐ)生(shēng)物合成等多條代謝途徑。研究發現(xiàn),通過4-BB刺激使細胞過表達PGC1α,可以維持線粒體(tǐ)的功能(néng)和避免TILs的耗竭,從而達到抗腫瘤效果;此外,PPAR-PGC1α激動劑與PD-1抗體(tǐ)聯合使用後,可以增加線粒體(tǐ)的生(shēng)物學活性。同時(shí)增加T細胞的抗腫瘤活性。
7. ACT中的代謝幹預措施
ACT療法在腫瘤治療中發揮着重要的作(zuò)用,但(dàn)是分(fēn)離的TILs屬于終末分(fēn)化(huà)細胞,因此生(shēng)存周期較短。但(dàn)是當TILs細胞内具有較高濃度的鉀離子(zǐ)時(shí),能(néng)夠抑制TCR驅動的AKT-mTOR信号,達到提高抗腫瘤能(néng)力的作(zuò)用。此外,CAR-T療法也(yě)是目前比較有前景的免疫療法。研究發現(xiàn),AKT和PI3K抑制劑可以改變CAR-T的代謝,增強其抗腫瘤效果。這(zhè)些(xiē)研究共同表明AKT-mTOR信号在促進T細胞終末分(fēn)化(huà)和活化(huà)中發揮重要功能(néng)(圖3)。
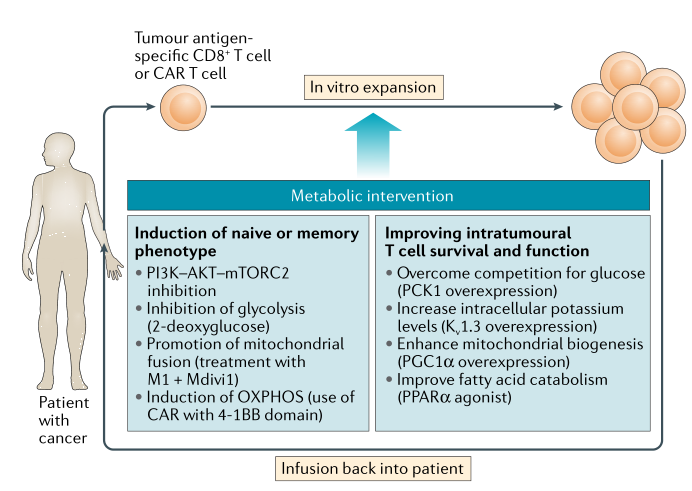
8. 總結
了(le)解腫瘤細胞和免疫細胞的代謝重編程如(rú)何調節抗腫瘤免疫反應,可以使我們在抗腫瘤免疫治療中尋找到合适的靶向代謝途徑的治療手段。因此,理(lǐ)解和利用TME中各種代謝的關(guān)系可以提高免疫療法的低(dī)應答(dá)率。值得注意的是,代謝編程也(yě)影響抗原的表達和識别。因此,代謝幹預不僅能(néng)夠改善免疫細胞對高免疫原性腫瘤的反應,而且能(néng)夠增加腫瘤細胞的免疫原性,從而擴大免疫療法治療的範圍。
